疾病诊断
童春容主任:什么是血液肿瘤的整合诊断?在临床中发挥着怎样的作用?
血液肿瘤的治疗是一个长期、精细的过程,其传统治疗方式主要包括手术、放疗、化疗、造血干细胞移植,近年来随着新药研发与临床探索的不断提速,靶向治疗、免疫治疗更是发挥出令人惊喜的效果,而如何进行精准整合诊断成为了其中重要的一环。本文中,北京高博博仁医院免疫与靶向治疗学科带头人童春容主任特别为广大血液病患者带来“血液肿瘤的整合诊断”的专业、精彩科普,帮助大家进一步了解整合诊断及其在临床治疗中至关重要的作用。

一、什么是整合诊断?
血液肿瘤包含多种类型,其诊断也是非常复杂,包括一系列实验数据和临床诊断。临床诊断需要整合患者的疾病史、家族史、药物毒物接触史、过敏史、传染病接触史等;实验室诊断包括MICM-PP等多种技术整合,并从临床诊断及治疗结果中不断修正、完善,提高诊断水平。临床诊疗最高的目标是治愈,其次是延长生命、改善生活质量、减轻患者痛苦。
01 血液肿瘤整合诊断需要回答哪些问题?
首先,是否有血液肿瘤细胞、比例是多少,以及血液肿瘤细胞的形态、组织病理、流式、染色体、基因等;其次是血液肿瘤细胞起源于哪种系列,以及预后分层,包括染色体、FISH、基因、治疗后MRD,以此来帮助选择合适的治疗方案;此外,还要帮助确定微小残留白血病(MRD)监测的标志,以及遗传易感基因或血液肿瘤前克隆(染色体、基因)等等。
02 现代诊断依赖MICM-PP整合诊断技术,MICM-PP是什么?
M——形态学+细胞化学、组织病理;
I——免疫组织化学、流式细胞分析(FCM)、免疫球蛋白电泳及定量;
C——细胞遗传、分子遗传(FISH)、CGH;
M——分子生物学:融合基因筛查及定量,基因多态性及基因突变(肿瘤基因、天生及遗传、药物代谢基因等),基因拷贝数分析,IgH/ TCR克隆性基因重排分析,病原基因,移植后供受者嵌合率;
P——病原学:病原基因、组织病原学、其它方法检测病原;
P——药物浓度及药物代谢基因组学。
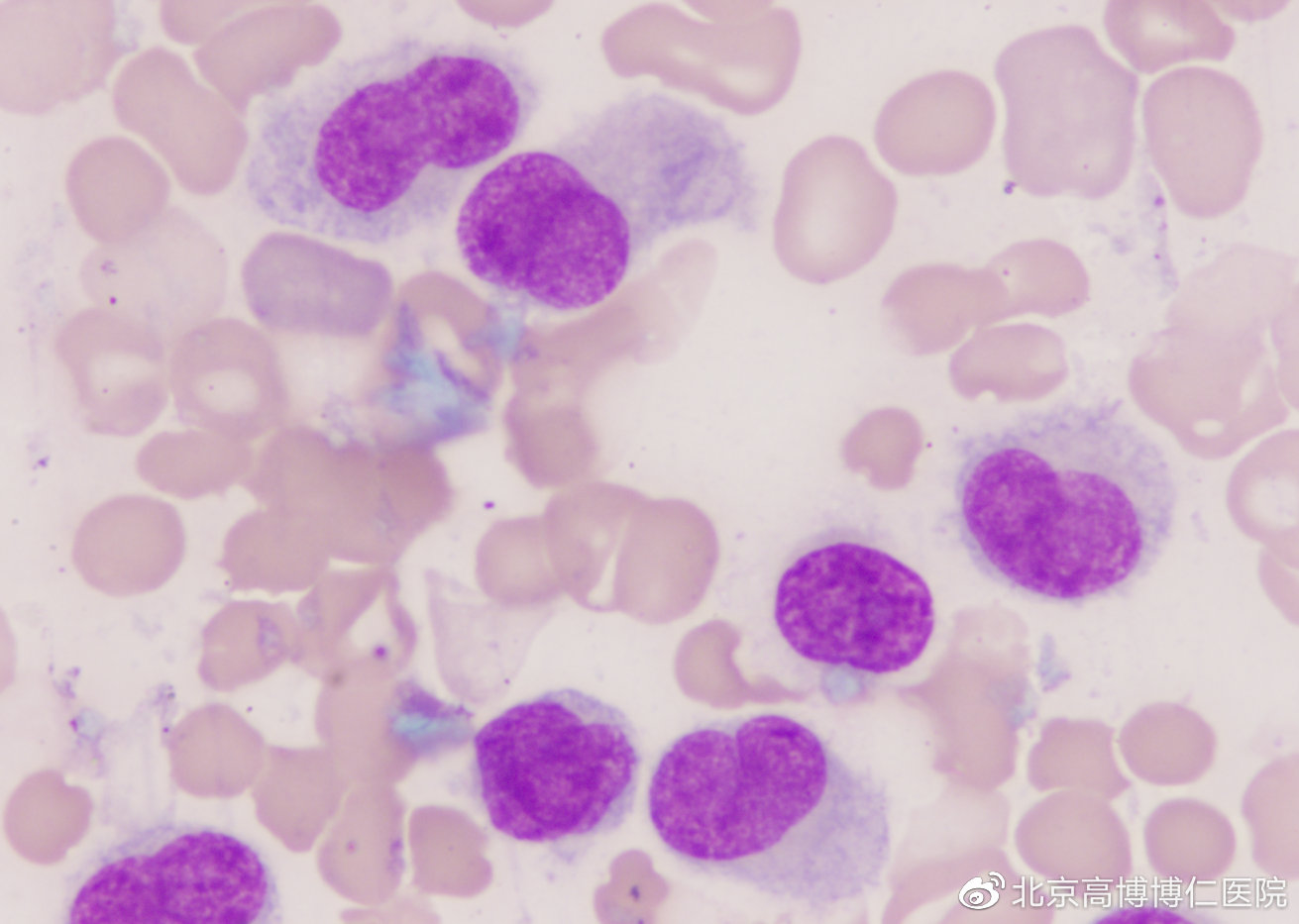
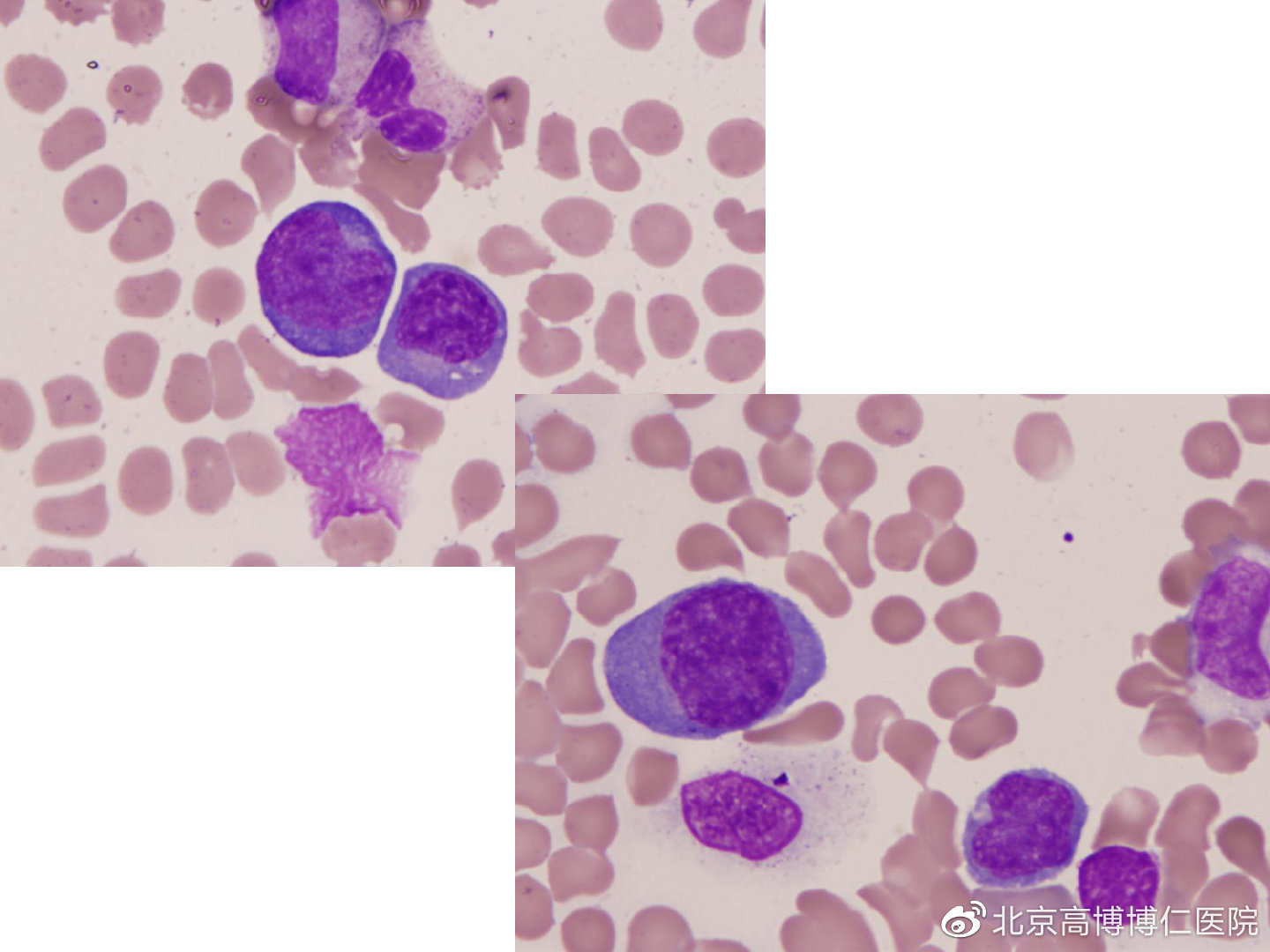
细胞形态及细胞化学分析的优点及缺点
细胞形态及细胞化学分析更加直观,一旦发现以下细胞判断为异常细胞,可立即确定或者缩小检查范围,优于其它方法。同时很少稀释,几乎未处理,因此确定目标细胞的比例更准确,对于医生来说,一些现象对医生有很好的提示价值,对于患者来说更加经济、快速。
其缺点在于,人为因素影响较大,仅根据形态学难以做出诊断及分类,比FCM更难以鉴别细胞的成熟阶段、来源系列、良恶性。此外,细胞形态及细胞化学分析的预后价值不如染色体及基因高。
病理及IHC的优点和缺点
病理及IHC的标本可以直接固定,不容易造成信息损失,恶性细胞比例更客观。对一些抽不出的、少见的、大细胞仍可诊断,如伴骨髓纤维化、多发性骨髓瘤(MM)、淋巴瘤、转移癌、组织细胞、巨噬细胞、树突细胞等,而且可以直接观察到组织结构,容易确定恶性细胞的组织部位。
但是病理及IHC诊断较慢、受诊断者个人经验及知识水平影响大,对一些组织结构无破坏、细胞形态改变不大的细胞,难以鉴定良恶性及成熟度;同时有些恶性细胞在液体中,难以获取组织标本,难以判断组织结构。
FCM的优点和缺点
FCM一次可检测数万至数十万个细胞上的数十种标记,可同时检测每个细胞的六个以上参数,敏感性高,分析全面,更容易区分良恶性,恶性细胞的成熟度及来源系列。同时可以帮助确定免疫治疗的靶点并监测疗效,如CD20、CD19、MHC分子等,是监测MRD覆盖面最广的方法。
但是FCM 不能确定组织结构,一些罕见的大细胞不能分析到,对霍奇金淋巴瘤(HL)等难以确诊。此外,标本需要尽快染色固定,尤其是穿刺、活检组织、体液标本,需要在4小时内染色;从抗体的选择、组合的配搭、分析都需要技术人员有丰富的知识和经验。
染色体的优点和缺点
染色体可以发现很多未知基因的染色体异常,有独立的诊断及预后价值。但是染色体诊断时间长,高度依赖诊断人员的丰富的技术、经验及知识水平。
FISH的优点和缺点
FISH有独立的诊断及预后价值,可以检测出显微镜下人眼难以分辨的染色体异常。细胞不分裂也能检测,分析的细胞数量比染色体多,且更能反映正常和恶性细胞的比例,监测残留白血病比染色体敏感;此外,诊断时间比染色体短,与染色体分析比较,对依断人员的经验依赖程度低。
但FISH探针昂贵,每次只能分析1-2种异常,且只能分析已知的染色体或基因异常。
基因检测的优点及缺点
基因检测有独立的诊断及预后价值,可以检测出染色体或FISH不能检测出的异常,联合染色体和FISH,增加了对疾病预后的判断能力,且诊断时间比染色体短;与染色体及FISH分析比较,对检测人员的经验依赖程度低。但基因检测对试验设计、试验、分析等过程的质量保证要求高。
基因检测在血液病诊治中的意义:
Ø 诊断价值
Ø 预后判断价值
Ø 基因变异指导的靶向治疗
Ø 药物代谢基因指导的个性化用药
Ø 基因指导的新抗原免疫治疗
Ø MRD, ctDNA监测指导的治疗
Ø 遗传性疾病的诊断
Ø 遗传易感基因与临床治疗的选择
Ø 多克隆及肿瘤前克隆
Ø 移植后供受者嵌合率
Ø 一些病原基因检测对病因了解有帮助:幽门螺旋杆菌、 HCV与淋巴瘤;EBV:淋巴系统疾病,噬血综合症(HLH)等;HHV8:Castleman 淋巴瘤;B19:血细胞减少;多种病毒与血液病相关,如AA、HLH、血细胞减少。
二、AL/LBL检验诊断的基本要求
AL/LBL检验诊断的基本要求是临床医生必须要掌握的:
1. 细胞形态+细胞化学染色;如果为LBL,肿块组织病理按病理协会相关要求;FCM;染色体。
2. FISH:染色体结果与基因检查不符合者,或染色体有难以确定的异常,或初诊融合基因定量<10%者,用FISH确认;
3. 基因:
Ø 包含有WHO(2016)AL重现性融合基因:RUNX1-RUNX1T1(AML1-ETO)、CBFB-MYH11、PML-RARA、MLLT3-KMT2A、DEK-NUP214、RPN1-EVI1、RBM15-MKL1、BCR-ABL、GATA2-MECOM、ETV6-RUNX1(TEL-AML1)、IL3-IGH、TCF3-PBX1(E2A-PBX1);
Ø 包含有WHO(2016)及NCCN指南AL基因变异检测:FLT3-ITD、NPM1、CEBPA、c-KIT、DDX41、RUNX1、ANKRD26、ETV6、GATA2基因变异;
Ø 对筛查阳性的融合或可定量的变异基因用荧光标记探针的Q-PCR或10万层以上深度测序定量,以备观察治疗效果。
AL/LBL检验诊断的较高要求多为新的进展:
Ø FISH:分别检查t(v;11q23)、t(v;5q31-33)、del(17p13)染色体异常。B-ALL/B-LBL:检查t(X/Y;14)(p22/p11;q32)、t(9q34;v)、t(5q31-33;v)、21号染色体内部扩增、t(14q23;v)、t(11q23;v)、t(19p13.3;v)染色体异常。
Ø 融合基因筛查:可以用多重巢氏PCR筛查几十种融合基因;还可以用二代测序检测靶基因范围内的任何融合基因。
Ø 基因变异筛查:帮助预后、靶向药、疗效监测,甚至新抗原免疫治疗。
Ø 血液肿瘤遗传易感基因:有家族史,尤其是患者需要移植,无非血缘供者,与选择供者及移植预处理方案。
Ø 对融合基因用定量PCR定量,对变异基因用几十万层以上深度测序定量,监测疗效、调整治疗。
Ø FCM:抗体或CART治疗的靶点。
Ø 药物代谢基因筛查:帮助选择化疗药及其剂量,减少副作用,提高疗效。
三、整合诊断病例分享
童春容主任用一个病例解释了整合诊断对于治疗决策的重要性。
病例回顾
患者女,20岁,复视4个月,头痛2个月,双下肢无力1月余,活动不能半个月。4月前出现视物成双水平位为重,2月患者再出现视物成双,伴有间断头痛,呕吐及双下肢无力,头颅MRI未见异常;CSF WBC 1110个/ul,考虑为“结脑”,予强烈抗痨治疗无效。
CSF:压力400mm H2O,WBC 8200个/ul,Mo 80%,葡萄糖0.6mmom/L,氯化物120 mmom/L,蛋白101mg/dL,涂片示“大量淋巴细胞”,仍考虑为“结脑”。
转至结核病医院继续抗结核治疗,心率曾降至30次/分,双下肢活动不能,每3小时需用一次脱水药。

(基因检测结果)
诊断:B淋巴母细胞淋巴瘤,并进行脑脊液染色体检查。

(BM染色体检查)
诊断后,判断患者为预后极差的B淋巴母细胞淋巴瘤,容易对化疗/放疗抵抗,故建议采用allo-HCT。
用MTX+Ida,Dex+L-ASP治疗后次日头疼消失,15日后下肢肌力恢复至基本正常。Allo-HCT后3月脑脊液、骨髓检查正常出院。该病例提示整合诊断对于治疗选择的重要性。
■ 本文专家介绍

高博医学(血液病)研究中心免疫与靶向治疗学科带头人,高博医学(血液病)北京研究中心北京高博博仁医院科研院长,血液一科(普通血液病)主任,从事血液内科临床工作及实验研究30多年。
擅长各类恶性血液肿瘤的整合诊断(整合临床病史及多种实验室诊断技术)及综合诊疗(化疗、免疫治疗、靶向治疗、中药等),注重个性化精准诊疗,尤其擅长血液肿瘤的免疫治疗。
为国内较早一批开展免疫治疗的专家之一,在CAR-T细胞治疗难治复发血液肿瘤领域为国际领先水平,获得国际学术界的认可。领导团队与企业合作联合在国内率先采用新型第二代CD19-41BB-CART CAR-T细胞治疗难治复发的急性B淋巴细胞白血病;此后联合开发了多种靶点的CART临床用于治疗血液肿瘤,包括CD1a、CD4、CD7、CD20、CD22、CD30、CD33、CD70、CD79b、CD123、CD138、CD371等。是国内外开展CART临床研究病例数及种类最多的中心治疗之一。多项研究成果在ASH、EHA,JSH上展示,多篇论文被《Leukemia》、《Blood Cancer Jour》等著名杂志收录。还注意发展多种免疫治疗技术,如新抗原免疫治疗等治疗血液肿瘤及实体瘤等。
- 标签:
- 血液一科(普通血液病)
- 童春容
- 血液一科
- 童春容





 京公网安备11010602050084号
京公网安备11010602050084号

